教育講演3
免疫不全症の新生児スクリーニング ∼熊本県の現況∼
国立病院機構熊本医療センター小児科 部長
水上 智之



教育講演3
国立病院機構熊本医療センター小児科 部長
水上 智之
 熊本県では2019年2月から免疫不全症の新生児スクリーニングを開始しましたので、説明します。
熊本県では2019年2月から免疫不全症の新生児スクリーニングを開始しましたので、説明します。
私たちの体の中には免疫をつかさどる様々な細胞や分子があり、病原体から体を守っています。それらが先天的に数的に不足したり、機能的異常があると、病原体に感染しやすくなり、その結果、生後間もないころから体重増加不良、肺炎、中耳炎などを発症しやすくなります。これが原発性免疫不全症です。
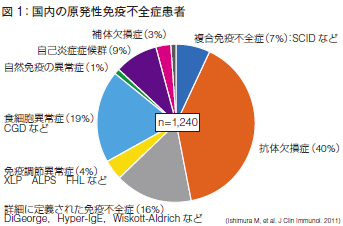
約10年前の国内の原発性免疫不全症患者の調査によると、患者数は1,240人で、発症頻度は4万人に1人という状況でした(図1)。現在は1万人に1人程度とも言われています。
一番多いのは4割を占める抗体欠損症です。そして、細胞性及び液性免疫不全を伴う複合免疫不全症が約1 割程度みられます。この中に重症複合免疫不全症(severe combined immunodeficiency:SCID)が含まれます。
 SCIDはT細胞の分化障害が主因で、細胞性免疫や抗体などの液性免疫が障害される疾患です。生後数ヵ月ぐらいから重症感染症、例えばPneumocystis、Aspergillus、サイトメガロウイルスなどの肺炎、慢性下痢、体重増加不良などを呈し、非常に予後不良な疾患で、造血幹細胞移植などをしなければ、1年以内に多くの患者さんが亡くなってしまう重症な疾患です。
SCIDはT細胞の分化障害が主因で、細胞性免疫や抗体などの液性免疫が障害される疾患です。生後数ヵ月ぐらいから重症感染症、例えばPneumocystis、Aspergillus、サイトメガロウイルスなどの肺炎、慢性下痢、体重増加不良などを呈し、非常に予後不良な疾患で、造血幹細胞移植などをしなければ、1年以内に多くの患者さんが亡くなってしまう重症な疾患です。
発症頻度はアメリカで約6万人に1 人、イギリスで約5万人に1人、台湾でもvariant タイプを含めると約6万人に1人といわれています。
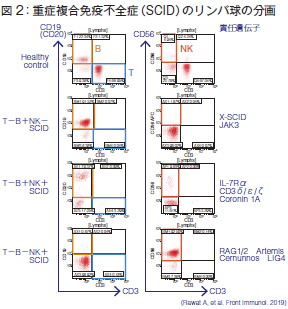
SCIDのリンパ球の分画をフローサイトメーターでみてみます(図2)。茶色で示しているのがB細胞、青で示しているのがT細胞、赤で示しているのがナチュラルキラー細胞です。SCIDではT細胞は全部に見られなくなっているのですが、B細胞、ナチュラルキラー細胞が残っているタイプあるいはないタイプなどの3つのタイプに分かれます。それぞれの責任遺伝子が決まっていて、よく知られているのはX染色体上の遺伝子異常によって起こるX-SCIDです。
SCIDが診断されると、早期に造血幹細胞移植を行います。一般に診断後早期3.5ヵ月以内の移植は良好で、それ以降であっても、感染症が落ちついた状況で移植をすると成績は良好となります。一方、感染症がまだ活動性の状態で移植すると、予後が不良となります。
活動性感染症がない状況であれば、移植する細胞種によってそれほど移植成績は変わらないのに対し、活動性感染症がある状況では、入れる細胞種により、予後が大幅に変わります。
ということで、できるだけ早期にSCIDの患者さんを診断して、移植に持ち込む、特に感染症の発症前に見つけることが重要で、新生児期にどうやって見つけるかというのが重要なテーマでした。
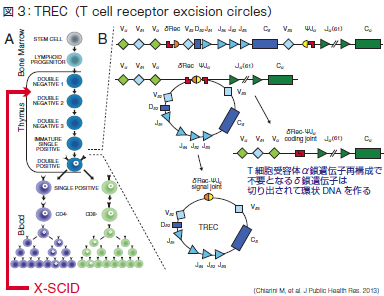 そこに出てきたのがTREC(T cell receptor excision circles)です。T細胞の表面にはα鎖、β鎖から成る受容体と、γ鎖とδ鎖から成る受容体があり、末梢血中にはα鎖、β鎖から成るαβT細胞が多くみられます。このT細胞が未熟な段階から胸腺で分化して、そして末梢に入り、抗原と出会って増殖していきます。
そこに出てきたのがTREC(T cell receptor excision circles)です。T細胞の表面にはα鎖、β鎖から成る受容体と、γ鎖とδ鎖から成る受容体があり、末梢血中にはα鎖、β鎖から成るαβT細胞が多くみられます。このT細胞が未熟な段階から胸腺で分化して、そして末梢に入り、抗原と出会って増殖していきます。
その過程で、表面上にT細胞受容体が発現する時、α鎖とδ鎖は対立遺伝子の関係にあります。α鎖が選択されると、要らなくなったδ鎖の一部分が切り出されて環状DNA(TREC)をつくります(図3)。α鎖はその後、細胞が増殖して、きちんと複製されますが、切り出された環状DNA(TREC)は複製されません。つまり、TRECがあれば、新生された未熟なT細胞数があることを反映しています。こうして、TRECがSCIDの診断マーカーに使えると考えられるようになりました。
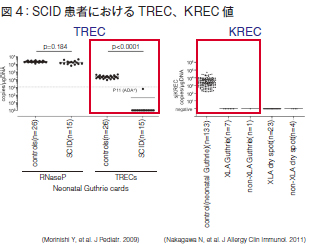 図4は今から10年ほど前に、東京医科歯科大学の今井耕輔先生らのグループが報告したもので、新生児のガスリーろ紙中の分子を調べると、健常者はTRECが十分あるのに対し、SCIDの患者さんでは著しく欠損していることがわかりました。
図4は今から10年ほど前に、東京医科歯科大学の今井耕輔先生らのグループが報告したもので、新生児のガスリーろ紙中の分子を調べると、健常者はTRECが十分あるのに対し、SCIDの患者さんでは著しく欠損していることがわかりました。
同様にB細胞表面上の免疫グロブリン鎖が同様に遺伝子再構成を起こしますので、表面上の遺伝子が発現するときに同じようにKREC (Kappa-chain recombination excision circles) と呼ばれる環状DNAが作られます。健常者では十分に存在するにもかかわらず、無γグロブリン血症の患者さんでは、KRECが著しく減少していることがわかりました。このTRECとKRECが免疫不全の新生児スクリーニングに用いられるようになってきました。
乾燥ろ紙血中のTREC値を定量PCRで測定する方法が、2008 年にアメリカウィスコンシン州の新生児スクリーニングで開始され、その後、世界に広がりました。
2017年には、日本では愛知県がスタートし、2019年2月に熊本県でもスタートしたという状況です。SCIDは以前は感染症などで診断されるか、あるいは家族にSCIDの患者さんがいて、次の出生児がSCIDであるかを診断するのが大半でした。現在は新生児スクリーニングによって、患者さんが見つかるようになってきました。つまり、感染症を起こす前に、できるだけ早期に患者を見つけることができるようになったわけです。
ただ、TRECがカットオフ値よりも少ないということでスクリーニングされても、その全てがSCIDというわけではありません。SCIDはそのごく一部です。
2014年、JAMAに掲載されたKwan らの報告によれば、SCID以外にも、DiGeorge 症候群、ダウン症候群、あるいは二次性疾患(先天性心疾患、消化管奇形、乳糜胸)などが含まれていました。
2019年の愛知県の報告でも、精査対象者48人中T細胞減少は11人で、DiGeorge、Wiskott-Aldrich、ダウン症候群などが含まれていました。これらを上手に鑑別してSCIDを見つけることが重要になります。
それでは、熊本県で開始された約1年分のSCIDの新生児スクリーニングを報告いたします。
【対象】熊本県内47の施設で出生して、検査に対する同意を得た新生児の血液ろ紙です。このろ紙はタンデムマスと同一のものです。現在はパイロットスタディ(無料)で行われています。
【期間】2019年2月から2020年3月までの約1年間分で検査は継続中です。
【方法】定量PCR/ ダイレクト法(1st )、抽出法(2nd)です。B細胞欠損症で著減するKRECの測定は行っていません。
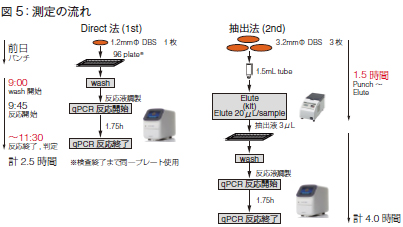 定量PCRの測定の流れを説明します(図5)。まず、ダイレクト法(1st)として、患者さんの血液を1.2mmΦでパンチアウトして、そのろ紙をプレート上に並べ、反応液と反応させ、実際に定量PCRを行います。
定量PCRの測定の流れを説明します(図5)。まず、ダイレクト法(1st)として、患者さんの血液を1.2mmΦでパンチアウトして、そのろ紙をプレート上に並べ、反応液と反応させ、実際に定量PCRを行います。
そして、抽出法(2nd)として、カットオフ値未満の患者さんの検体として、今度は3.2mmΦでパンチアウトしたろ紙からDNAを抽出して、その抽出DNAでもう一度定量PCRを行って、TRECを測定します。
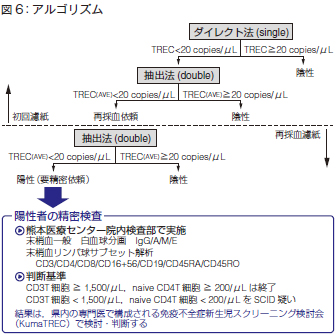 図6がアルゴリズムです。まず、ダイレクト法で20copies 未満の方ついては抽出したDNAで再検を行い、さらに20copies 未満の方に再採血を依頼します。新しく寄せられたろ紙の中からもう一度DNAを抽出し、20copies 未満の方(陽性者)を我々の病院でフローサイトメーターなどで再検査するということになります。ここまでが約1ヵ月弱です。
図6がアルゴリズムです。まず、ダイレクト法で20copies 未満の方ついては抽出したDNAで再検を行い、さらに20copies 未満の方に再採血を依頼します。新しく寄せられたろ紙の中からもう一度DNAを抽出し、20copies 未満の方(陽性者)を我々の病院でフローサイトメーターなどで再検査するということになります。ここまでが約1ヵ月弱です。
陽性者の精密検査は、熊本医療センター院内検査部で実施します。まず、血液検査で末梢血一般、白血球分画、IgG/A/M/Eなどの免疫グロブリン、末梢血リンパ球サブセット解析を行います。
そして、CD3T細胞≧1500 /µL、naiveCD4T細胞≧200/µLの場合は恐らく問題がないであろうということで、ここで一旦精査は終了となります。
CD3T細胞<1500 /µL、かつnaiveCD4T細胞<200/µLの場合にはSCIDを疑って、さらに厳密な管理治療に進み、SCIDより軽度なT細胞減少症の場合でも引き続き精査を続けていく流れで進めています。結果は、県内の専門医で構成される免疫不全症新生児スクリーニング検討会(KumaTREC)で検討・判断しています。
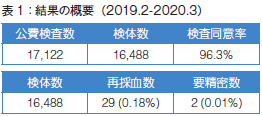 1年分のSCIDの新生児スクリーニング結果の概要です(表1)。
1年分のSCIDの新生児スクリーニング結果の概要です(表1)。
これまでに16,488 検体を解析し、再採血までに至ったのが29検体(0.18%)、さらに要精密で当院にいらした方が2名(0.01%)でした。TRECのコピー数は平均で102copies/µLで、カットオフ値20未満の数字を出した方が29名(0.18%)ということでした。
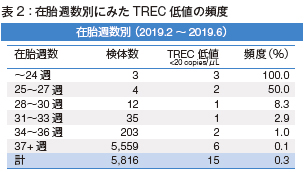 表2は昨年6月までの約5ヵ月間のデータですが、この段階でTRECが低かった方が15名いて、その方々の在胎週数を見てみますと、24週未満では100%TRECが低く、25~27週で50%でした。在胎週数が若いほどTRECが低いことがわかりました。これは従来の報告と同一です。
表2は昨年6月までの約5ヵ月間のデータですが、この段階でTRECが低かった方が15名いて、その方々の在胎週数を見てみますと、24週未満では100%TRECが低く、25~27週で50%でした。在胎週数が若いほどTRECが低いことがわかりました。これは従来の報告と同一です。
出生時体重別でも、やはり体重が軽い方のほうが、TRECが低いことがわかりました。こうした結果から、現在、早産で測定した方に関しては37週で再検査をして評価する方法を行っています。
最終的に当院で2例、精密検査を行いました。1例目は既にわかっていましたがMiller-Dieker 症候群の方で、この方はT細胞減少なし、免疫グロブリン値も正常で現在経過観察をしております。もともとMiller-Dieker 症候群は脳の奇形あるいは顔面の異常などを伴っており、過去に1例だけT細胞減少症の報告はありましたが、この方はそれに該当しませんでした。
もう1例、T細胞減少症が見つかりました。この方はCD3T細胞が590/µL、naiveCD4Tが202/µLと非常に少なかったのですが、現在、経過観察中にT細胞が増加傾向にありまして、状態が落ちついています。念のため、SCID遺伝子パネルにも載せまして、染色体分析も行いましたが、現在のところ、著しい異常は見つかっていません。注意深く経過を見ているところです。
●熊本では2019 年2 月から、定量PCR法によるTREC 測定を用いた免疫不全症新生児スクリーニング検査を開始しました。
●2020 年3 月末までの16,488 検体の解析では、TREC 測定値は平均102.5copies/µLでした。TREC 低値による再採血依頼は29 例(0.18%)で、在胎週数の短い児がその大半を占めました。
●要精密は2 例(0.01%)でした。
1例はMiller-Dieker 症候群の女児で、精査でT細胞減少症は認められませんでした。別の1 例はT 細胞減少症として精査・管理中です。
 現在はパイロットスタディとして無料で実施していますが、来年以降は有償化を考慮しています。また、KRECは現在測定していませんが、今後測定するかを検討します(表3)。
現在はパイロットスタディとして無料で実施していますが、来年以降は有償化を考慮しています。また、KRECは現在測定していませんが、今後測定するかを検討します(表3)。
カットオフ値に関しては、現在20copies/µLの設定です。当初、1年間で現在の10倍ぐらい精査対象者が出ると予測していましたが、予想よりも非常に少ない患者数となりました。今後この値を上げてしまうと、偽陽性が出てしまう可能性があります。逆に下げてしまうと、今度は非典型SCIDや時々こういうスクリーニングで出てくるWiskott-Aldrich のような、非常に重要な免疫不全症を見逃す可能性もあります。このあたりは他県の検査結果や患者数等を見ながら、再検討していく部分と考えています。
 もう1つの重要な検討事項は、2020年10月から始まるロタウイルスワクチンの予防接種への影響です(表4)。10月から定期接種化されますが、ロタウイルスワクチンの定期接種の対象者から除外される者として、「SCIDの所見が認められる者」と記載されています。過去にも世界からSCIDが診断される前に既にロタウイルスワクチンを接種されて、そしてそのワクチン株に感染して慢性下痢を起こしたり、重度の体重増加不良を来した方々の報告がありました。こういう方々には接種しないで、見つけ出して回避していくステップが必要になります。
もう1つの重要な検討事項は、2020年10月から始まるロタウイルスワクチンの予防接種への影響です(表4)。10月から定期接種化されますが、ロタウイルスワクチンの定期接種の対象者から除外される者として、「SCIDの所見が認められる者」と記載されています。過去にも世界からSCIDが診断される前に既にロタウイルスワクチンを接種されて、そしてそのワクチン株に感染して慢性下痢を起こしたり、重度の体重増加不良を来した方々の報告がありました。こういう方々には接種しないで、見つけ出して回避していくステップが必要になります。
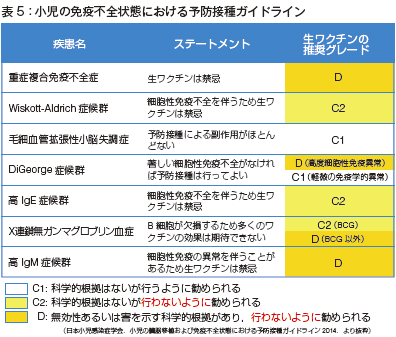
2014年に日本小児感染症学会が、このような免疫不全状態における方々の予防接種ガイドラインを作成し、無効性あるいは害を示す科学的根拠があり、行わないように勧められる疾患(D)を設定しています。その中にSCID、DiGeorge症候群(高度細胞性免疫異常を伴う)、高IgM症候群、X連鎖無ガンマグロブリン血症などが含まれます(表5)。
他にも、科学的根拠はないが行わないように勧められる疾患(C2)としてWiskott-Aldrich あるいは高IgE症候群などもあります。SCIDのスクリーニングで見つかってくるこのような患者さんでは、できるだけ早期に診断して、これらの生ワクチンを回避していくことが今後重要になると思われます。
●1年間で1万6000 人以上の新生児スクリーニングが行われ、2例の陽性者が出ています。
●今後もこの検査を継続して、カットオフあるいは検査の有用性の評価等を行います。
●2020 年10 月からロタウイルスワクチンが定期化されます。このようなワクチンを接種すべきでないとされる免疫不全症の児を早期に見つけて、ワクチンを回避していく上ではスクリーニング検査は有用な手段になるのではと考えています。
坂本:治療は造血幹細胞移植になるようですけれども、この造血幹細胞移植は3.5ヵ月以内のほうが予後がよいとされています。SCIDのスクリーニングをすることで、治療に踏み込める時期というのは、生後1~2ヵ月とか、大分早くできるのでしょうか。
水上:早期に見つかることによって、移植の時期も診断も早くなれば、ドナーの選定、そして、移植を行う施設の決定など、全てのステップが早期に進むようになれば、移植も非常に早い段階で終わるようになります。今までは診断がついてから治療をコントロールしながら移植に進んでいたので、現場の先生方の苦労も非常に多かったと思います。そういうことが少しでも軽減できるということは、全てに対して非常にメリットが出てくると思います。

教育講演1・教育講演2 座長
熊本大学大学院生命科学研究部小児科学講座 准教授
松本 志郎

教育講演1
熊本大学大学院生命科学研究部小児科学講座 教授
中村 公俊

教育講演2
熊本大学大学院生命科学研究部小児科学講座
澤田 貴彰

教育講演3・教育講演4 座長
熊本大学病院総合周産期母子医療センター 講師
坂本 理恵子

教育講演3
国立病院機構熊本医療センター小児科 部長
水上 智之

教育講演4
宮崎大学医学部看護学科 基礎看護学領域 教授
宮崎大学医学部附属病院小児科
宮崎県新生児マススクリーニング検査専門委員会 委員長
澤田 浩武

特別講演 座長
熊本大学大学院生命科学研究部小児科学講座 教授
中村 公俊

特別講演
公益財団法人 ちば県民保健予防財団 調査研究センター長
羽田 明

熊本大学大学院生命科学研究部小児科学講座 教授
中村 公俊